| Themen-Auswahl | ENERGIE-WISSEN | Leitseite |
 |
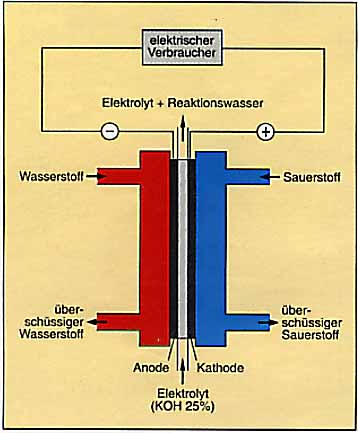
Schema einer BrennstoffzelleDie Brennstoffzelle verwandelt chemische Energie in Strom |
Brennstoffzellen erzeugen Strom aus Wasserstoff und Sauerstoff, wobei in unterschiedlichem Ausmaß auch Wärme anfällt und als "Abfallprodukt" Wasser entsteht. Wie Batterien und Akkumulatoren gehören sie zu den elektrochemischen Energiewandlern, die man auch als "galvanische Elemente" bezeichnet. Im Unterschied zur Batterie ist aber der Energievorrat, aus dem sie den Strom erzeugen, nicht in der Zelle gespeichert, sondern wird kontinuierlich von außen zugeführt. Sie können deshalb so lange Strom erzeugen, wie die Zufuhr von Wasserstoff und Sauerstoff andauert.
Die ersten praktisch nutzbaren Brennstoffzellen wurden für den Einsatz in U-Booten und Raumfahrzeugen entwickelt. Bei den Mondlandungen im Rahmen des Apollo-Programms deckten Brennstoffzellen den Strombedarf des Raumschiffs und lieferten zugleich das Trinkwasser für die Astronauten. Heute arbeitet man daran, Brennstoffzellen als Energielieferanten für Elektroautos, als Kraftwerke für die Stromversorgung und für viele andere Zwecke einzusetzen.
Im Prinzip bestehen alle Brennstoffzellen aus zwei porösen Flächen (Elektroden), die durch eine dritte Fläche (Elektrolyt) voneinander getrennt sind. An die eine Elektrode wird Wasserstoff herangeführt, an die andere Sauerstoff. Ohne den Elektrolyten würden sich beide Gase vermischen: Es käme dann allenfalls zu einer normalen Verbrennung bzw. zu einer Knallgasreaktion. Der Elektrolyt bewirkt jedoch statt der normalen Verbrennung eine elektrochemische Reaktion: An der einen Elektrode (Anode) bilden sich positiv geladene Wasserstoff-Ionen und an der anderen Elektrode (Kathode) negativ geladene Sauerstoff-Ionen. Dadurch entsteht eine elektrische Spannung zwischen den beiden Elektroden, wie zwischen den Polen einer Batterie. Und wie bei dieser läßt sich diese Spannung praktisch nutzen, wenn man die Elektroden über einen äußeren Stromkreis miteinander verbindet.
Wie alle galvanischen Elemente erzeugen Brennstoffzellen Gleichstrom. Die Spannung pro Zelle beträgt je nach Typ etwa ein Volt. Diese "Leerlauf"-Spannung sinkt allerdings mehr oder weniger stark, sobald ein nennenswerter Strom fließt. Man muß deshalb einen Kompromiß zwischen Stromstärke und Spannung finden. In der Regel betreibt man die Zellen bei einer Spannung von 0,7 Volt.
Um höhere Spannungen und Leistungen zu erzielen, fügt man die einzelnen Zellen in Serien- oder Parallelschaltung zu Stapeln zusammen. Diese Zellstapel werden mit einem englischen Ausdruck auch als "stacks" bezeichnet. Wenn von "der" Brennstoffzelle als Stromlieferant die Rede ist, meint man immer eine Vielzahl gleichgearteter Zellen, die in Form von "stacks" zu der gewünschten Leistungseinheit vereinigt wurden. Die Netzeinspeisung oder die Versorgung von Wechselstrom-Geräten erfolgt über einen Wechselrichter.
Die ideale Brennstoffzelle verwandelt die chemische Energie der Brenngase hundertprozentig in Strom. Man spricht deshalb auch von einer "kalten Verbrennung", um den Unterschied zur normalen Verbrennung zu betonen, bei der aus der chemischen Reaktion des Brennstoffs mit dem Luftsauerstoff lediglich Wärme als vergleichsweise minderwertige Form von Energie entsteht. In der technischen Praxis geht es aber nicht ganz so ideal zu: Je nach Typ braucht die Brennstoffzelle für die elektrochemische Energiewandlung eine Betriebstemperatur von 60°C bis zu über 1000°C. Als Faustregel kann gelten. Alle Brennstoffzellen erzeugen deshalb nicht nur Strom, sondern auch Wärme. Dies wirkt sich naturgemäß zu Lasten ihres elektrischen Wirkungsgrades aus. Die energetische Bilanz verbessert sich jedoch, wenn man die Brennstoffzelle z.B. als Blockheizkraftwerk betreibt, das gleichzeitig Strom und nutzbare Wärme liefert. Bei Hochtemperatur-Brennstoffzellen läßt sich mit der Abwärme auch ein nachgeschaltetes Gas- und Dampfturbinenkraftwerk betreiben und so der elektrische Wirkungsgrad erhöhen.
 |
Den grundsätzlichen Aufbau einer Brennstoffzelle veranschaulicht dieses Demonstrationsmodell vom Typ PEMFC, das für Unterrichtszwecke entwickelt wurde und deshalb zerlegt werden kann: Auf den beiden siebförmigen Blechen sind die Elektroden angebracht (Kohlefilz mit Platin als Katalysator). Zwischen den Elektroden-Blechen befindet sich der Elektrolyt in Form einer festen Kunststoffmembran. Die Demo-Zelle hat im Leerlauf eine Spannung von 0,9 Volt und kann einen dazugehörigen winzigen Motor mit 20 Milliwatt in Drehung versetzen. - Normale Brennstoffzellen setzen sich aus einer Vielzahl solcher einzelnen Elemente zusammen, die durch Serien- oder Parallelschaltung zur gewünschten Leistungsgröße vereinigt werden. |